- 当前位置:首页 > 休闲 > 牛奶中吡利霉素残留检测方法——高效液相色谱一串联质谱法(一)
游客发表
1、牛奶安全要求
实验操作时穿工作服、中吡戴口罩和手套;提取和净化操作都应在通风橱中进行,利霉留检联质避免溶剂气体吸人和皮肤接触;废弃的素残化学试剂收集到专用容器中集中处理。
2、测方急救措施
皮肤接触到有机溶剂或酸、法高碱溶液后用清水清洗,效液相色有机溶剂或酸、谱串谱法碱溶液溅人眼中用清水灌洗。牛奶
3、中吡适用范围
该标准操作规程适用于牛奶中吡利霉素残留量的利霉留检联质确证检测。
4、素残职责
进行该项检验的测方检验员必须按该标准操作规程进行检验,质量监督员负责监督该标准操作规程的法高正确执行。
5、效液相色原理
试料中残留的毗利霉素用1%甲酸乙腈溶液提取,MCX固相萃取柱净化,氮气吹干浓缩,以高效液相色谱一串联质谱法测定,异吡利霉素作内标,内标法定量。
6、方法灵敏度
吡利霉素在牛奶中的检出限为2μg/kg,定量限为5μg/kg。
7、注意事项
在固相萃取预洗、淋洗和洗脱过程中应注意流速,不能过快或过慢。
8、材料、仪器、试剂的准备及基本要求除特别注明外,以下所用试剂均为分析纯;水为符合GB/T 6682规定的一级水。
8.1 对照品、试剂和药物储备液、工作液准备;
8.1.1 吡利霉素对照品 含C17H31ClN2O5S不得少于97.0%;
8.1.2 异吡利霉素对照品 含C17H31ClN2O5S不得少于94.0%;
8.1.3 甲酸;
8.1.4 乙腈 色谱纯;
8.1.5 正丙醇;
8.1.6 乙酸铵;
8.1.7 甲醇 色谱纯;
8.1.8 1%甲酸的50mmol/L乙酸铵溶液 取乙酸铵0.77g,置200mL量瓶中,加2mL甲酸,用水溶解稀释至刻度,摇匀即得。
8.1.9 1%甲酸乙腈溶液 量取1mL甲酸,置100mL量瓶中,用乙腈稀释并定容,摇匀即得。
8.1.10 2%甲酸水溶液 量取2mL甲酸,置100mL量瓶中,用超纯水稀释并定容,摇匀即得。
8.1.11 5%氨水甲醇溶液 量取5mL氨水,置100mL量瓶中,用甲醇稀释并定容,摇匀即得。
8.1.12 吡利霉素标准储备液(1mge/mL) 精密称定盐酸吡利霉素对照品约11.23mg,置10mL棕色量瓶中,用甲醇溶解并稀释成浓度为1mg/mL的标准储备液。-20%以下保存,有效期为3个月。
8.1.13 异吡利霉素内标储备液(1mg/mL) 精密称定盐酸异吡利霉素对照品约11.59mg,置10mL棕色量瓶中,用甲醇溶解并稀释成浓度为1mg/mL,-20℃以下保存,有效期为3个月。
8.1.14 标准工作液配制(1μg/mL) 准确量取0.1mL标准储备液,置于10mL量瓶中,用甲醇稀释并定容,即成10μg/mL吡利霉素标准工作液;从中量取1.0mL,置于10mL量瓶中,用甲醇稀释并定容,摇匀即得lμg/mL吡利霉素标准工作液。-20℃以下保存,有效期为1个月。
8.1.15 内标工作液配制(1μg/mL) 准确量取0.1mL内标储备液,置于10mL量瓶中,用甲醇稀释并定容,即成10μg/mL内标工作液;从中量取1.0mI。内标工作液,置于10mL量瓶中,用甲醇稀释并定容,摇匀即得1μg/mL的内标工作液。-20℃以下保存,有效期为1个月。
8.2 仪器和设备;
8.2.1 高效液相色谱-串联质谱仪(配电喷雾离子源);
8.2.2 天平感量0.01g;
8.2.3 分析天平 感量0.00001g;
8.2.4 涡旋混合器;
8.2.5 离心机;
8.2.6 旋转蒸发仪;
8.2.7 氮吹仪;
8.2.8 离心管50mI。
8.2.9 微孔滤头0.45μm;
8.2.10 鸡心瓶,50mL;
8.2.1l 固相萃取装置;
8.2.12 MCX固相萃取柱(60mg/3mL),或相当者。
9、检验步骤
9.1 试料的制备;
9.1.1 取新鲜或解冻的供试样品,作为供试试料。
9.1.2 取新鲜或解冻的空白样品(2±0.02)g,作为空白试料。
9.1.3 取新鲜或解冻的空白样品(2±0.02)g,添加1斗∥mL标准工作液0.2mL,作为空白添加试样(阳性对照)。
9.2提取
9.2.1 取试料(2±0.02)g,置50m1.离心管,加入内标工作液0.2mL,再加入1%甲酸乙腈溶液5mL,涡旋混合提取10s,5000r/min离心5min,转移上清液至50mL鸡心瓶。
9.2.2 离心管中的沉淀物用l%甲酸乙腈溶液5mL重复提取1次,合并上清液,加正丙醇3mL,于50℃真空旋转蒸发至干。
9.2.3 残余物用含1%甲酸的50mmol/L乙酸铵溶液5mL溶解,备用。
9.3 净化
9.3.1 MCX小柱依次用甲醇、水各3mL预洗。
9.3.2 取全部备用液过柱。
9.3.3 用2%甲酸水溶液、甲醇各3mL淋洗,减压抽干。
9.3.4 用5%氨水甲醇溶液3mL洗脱,抽干,洗脱液全部回收。
9.3.5 洗脱液于60%氮气下吹干。残余物用1.0mL甲醇溶解,摇匀,经微孔滤头过滤后,供高效液相色谱一串联质谱仪测定。
9.4 测定
9.4.1 色谱条件;
9.4.1.1 色谱柱:XBridge C18150mm×2.1mm(i.d.),粒径5μm,或相当者;
9.4.1.2 流动相:乙腈+0.0lmol/L乙酸铵(30+70,v/v);
9.4.1.3 流速:0.2mL/min;
9.4.1.4 柱温:30℃;
9.4.1.5 进样量:10μL。
9.4.2 质谱条件
9.4.2.1 离子源参考参数,电喷雾离子源(ESI+),毛细管电压为3.4 kV,锥孔电压为34 V,萃取电压为3 V,RF透镜电压为lV;源温为105℃,脱溶剂温度为350℃;锥孔气流速为50 L/h,雾化气流速为450L/h。
9.4.2.2质量分析器参考参数见表。
9.4.2.3光电倍增器电压:650V。
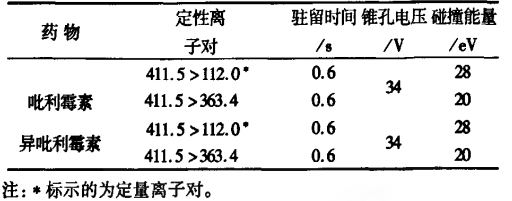
9.4.2.4定性、定量离子对、锥孔电压和碰撞能量见表。
参考资料:兽药残留检测标准操作规程,版权归原作者所有,如涉及作品内容、版权等问题,请与本网联系。
相关链接:试剂,吡利霉素,异吡利霉素,乙酸铵
随机阅读
热门排行
