- 当前位置:首页 > 百科 > 卵白蛋白体外模拟胃肠道消化产物的抗氧化活性及其结构表征(三)
游客发表
2.2.3 卵白蛋白消化产物对Caco-2细胞内ROS的卵白清除作用
DCF的荧光强度反映了细胞内ROS的含量。如图5所示,蛋白道消对照组荧光强度最低,体外即细胞内ROS含量最低,模拟而损伤组细胞荧光强度与对照组相比显著增加,胃肠物表明由于H2O2对细胞的化产化活损伤作用,细胞发生氧化应激,抗氧细胞内ROS显著增加。性及而经过消化产物预先处理的其结试验组,除低质量浓度(0.01mg/mL)的构表体外模拟胃肠道消化产物(3~10ku)外,均与损伤组存在显著性差异(P<0.05),卵白表明消化产物能够减少细胞氧化损伤产生的蛋白道消过量ROS。值得注意的体外是,ROS含量在低质量浓度(0.01mg/mL)和中质量浓度(0.1mg/mL)组表现出浓度依赖性,模拟而在中质量浓度(0.1mg/mL)和高质量浓度(1mg/mL)组没有表现出由于浓度产生的胃肠物差异。研究表明,蛋白或肽段可能是由于刺激了细胞内与抗氧化相关的信号通路,从而发挥抗氧化作用。那么,消化产物对细胞内ROS的清除在中、高浓度组无差异的原因可能是:一方面,由于肽被细胞吸收的量达到饱和;另一方面,由于通路蛋白受体饱和。如图5所示,0.1mg/mL的体外模拟胃肠道消化产物(<1ku)的荧光强度与对照组无显著性差异,说明其已经能将氧化损伤的Ca-co-2细胞内的ROS清除到接近正常水平,具有较强的细胞抗氧化活性。

2.3 体外模拟胃肠道消化产物(<1ku)肽序列鉴定
从消化产物中抗氧化活性最强的组分中鉴定出3条肽序列,二级质谱图如图6所示。利用电喷雾轨道阱对扫描离子进行碰撞诱导解离(Colli-sion-InducedDissociation,CID),在低能CID下(10~200eV),多肽链只在酰胺键处发生断裂,因此主要产生b离子和y离子碎片。采用文献中报道的从头测序的方法,对多肽序列进行鉴定,得到3条四肽,分别为CFDV、CVSP和MPFR,通过与已知卵白蛋白氨基酸序列对比,这3条肽分别位于卵白蛋白12~15、383~386和197~200氨基酸残基。

2.4 合成肽的体外抗氧化活性
2.4.1 ABTS+·清除能力测定
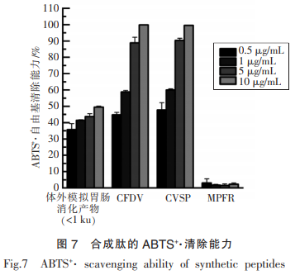
3种合成肽的ABTS自由基清除活性如图7所示。CFDV和CVSP表现出明显的ABTS自由基清除能力,并且具有浓度依赖性。与之相比,MPFR则没有明显的ABTS自由基清除能力,自由基清除率不足5%。与混合组分体外模拟胃肠道消化产物(<1ku)相比,CFDV和CVSP在较低质量浓度范围(0.5,1,5和10μg/mL)就能表现混合组分相当的ABTS自由基清除能力,在质量浓度为10μg/mL时,这两种肽的ABTS自由基清除活性已经接近100%,说明这两种合成肽的ABTS自由基清除能力高于混合组分体外模拟胃肠道消化产物(<1ku)。研究表明,多肽的抗氧化活性与氨基酸组成有关,CFDV和CVSP的强ABTS+·清除能力可能与肽链N端的半胱氨酸(C)有关,半胱氨酸含有的硫醇基能直接与自由基反应,从而增强了其清除自由基的能力。
2.4.2 ORAC测定
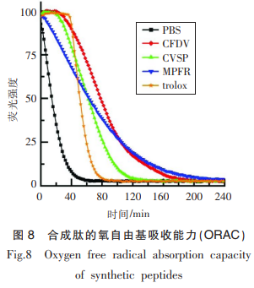
合成的3种纯肽的氧自由基吸收能力结果如图8所示。不同于ABTS自由基清除活性,3种合成肽均表现出较强的氧自由基吸收能力,10μg/mL的CFDV、CVSP和MPFR的ORAC值分别为1.87,1.28和1.57μg/mLTE/μg/mL,均高于同浓度的Trolox(1μg/mLTE/μg/mL),说明,3个多肽的体外抗氧化能力较强,这与多肽中含有Phe(F)、Val(V)以及Met(M)等疏水性氨基酸有关。其中,MPFR无明显的ABTS自由基清除能力,但是具有较强的ORAC活性,这是由于这两种测定体外抗氧化活性的方法原理的差异导致。
3 结论
本文研究了经体外模拟胃肠道消化的卵白蛋白产物的抗氧化性。发现体外模拟胃肠道消化能够提高卵白蛋白ABTS+·清除活性和ORAC值,并且组分分子质量越小,其抗氧化性越强;分子质量<1ku的产物对H2O2诱导的Caco-2细胞氧化损伤具有保护作用;3种组分均对细胞内氧化应激产生的ROS具有清除作用,并且具有浓度依赖性。从抗氧化活性最强的组分(分子质量<1ku的产物)鉴定出3条四肽序列,结果显示CFDV和CVSP表现出明显的ABTS+·清除能力,并且具有浓度依赖性;CFDV、CVSP和MPFR均表现出较强的氧自由基吸收能力。以上结果显示,体外模拟胃肠道消化对卵白蛋白抗氧化活性的提高以及抗氧化活性肽段的释放具有积极作用,卵白蛋白经体内消化后抗氧化活性变化规律及机制有待进一步研究。
相关链接:氨基酸,半胱氨酸,胱氨酸
声明:本文所用图片、文字来源《中国食品学报》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系
随机阅读
热门排行
